Новая технология позволила получить двухслойные трубки из живых клеток разных типов, аналогичные важнейшим слоям живого кровеносного сосуда. Даже отдельные клетки в них ориентированы в нужном направлении, без чего такой сосуд не сможет работать в теле.

Заменить поврежденный сосуд на искусственный, сделанный из биосовместимых полимеров, возможно далеко не всегда. Прежде всего это касается сосудов, которые обеспечивают кровоснабжение сердца. Поэтому ученые ищут методы, позволяющие вырастить настоящий, полноценный многослойный сосуд из клеток пациента. Важный прорыв в этом направлении удалось сделать команде из Мельбурнского университета, получившей полую трубку из нескольких слоев живых клеток, собранных так же, как в настоящем сосуде. О работе рассказывается в статье, опубликованной в журнале ACS Applied Materials and Interfaces.
Многие больные нуждаются в замене поврежденных кровеносных сосудов. Вместо крупных сегодня можно использовать синтетические трубки. Однако для средних и мелких сосудов (в том числе для коронарных, снабжающих кровью сердце) этот подход не работает: искусственные полимеры быстро «обрастают» тромбами, блокирующими просвет. В таком случае можно позаимствовать не столь важный сосуд из другой части тела и трансплантировать его. Но найти подходящий удается не у всякого пациента.
Идеальным решением могла бы стать технология выращивания живых сосудов из собственных клеток больного. Однако полноценно решить эту задачу пока не удается. Кровеносный сосуд — сложная, многослойная структура, работа которой зависит в том числе от корректной ориентации каждой клетки.
Внутренний слой состоит из клеток эндотелия, образующих волокна, идущие вдоль оси сосуда. Они облегчают ток крови и препятствуют возникновению тромбов. Его окружает промежуточный слой гладкой мускулатуры, клетки которой ориентированы перпендикулярно оси, образуя кольца. Они контролируют диаметр сосуда, регулируя кровоток. Наконец, внешний слой соединительной ткани придает целостность и упругость всей структуре.
Современные технологии позволяют выращивать клетки нужной ткани. Однако ключевой проблемой в получении искусственных сосудов остается правильная ориентация клеток в каждом слое. Решить ее удалось профессору Андреа О’Коннор (Andrea O’Connor) и ее коллегам из Мельбурнского университета.
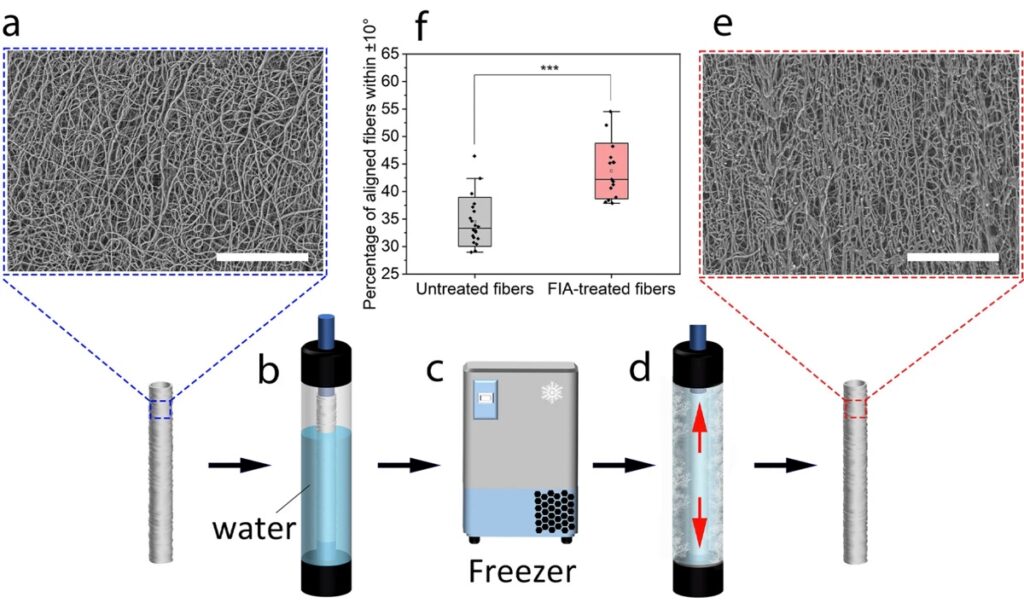
Чтобы получить трубчатую основу для выращивания клеток, ученые применили электроспиннинг — вытягивание тончайших полимерных нитей из жидкой струи под действием электрического поля. Такие нити наматывали на катушку из биоразлагаемого поликапролактона. Проблема в том, что этот подход не позволяет контролировать ориентацию нитей на катушке, и они накручиваются, хаотически меняют направление. Выращенные на такой поверхности клетки эндотелия также ориентируются случайно.
Поэтому О’Коннор с соавторами помещали катушку в трубку с водой и замораживали ее. Возникающие в таких условиях кристаллы льда преимущественно ориентированы вдоль оси трубки, и их появление «расправляет» нити полимера, придавая им то же базовое направление. Это направление — вдоль оси будущего сосуда — получали и эндотелиальные клетки, выращенные на такой подложке.
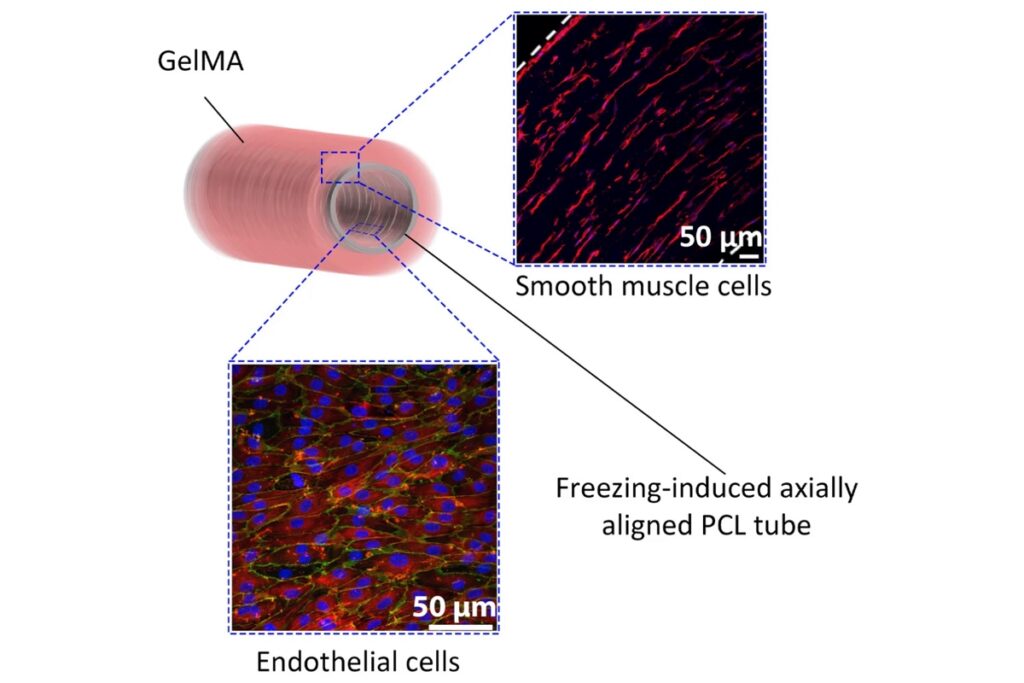
Далее их покрывали слоем гидрогеля — полимера, насыщенного водой. Используя гель с определенной (довольно высокой) мягкостью, ученым удалось добиться того, что выращиваемые на нем мышечные клетки формировали кольца, идущие поперек оси «сосуда». Наконец, слой полимерных нитей и гидрогель естественным образом деградируют.
Авторы статьи подчеркнули, что пока новая технология не позволяет получать полноценные, готовые к трансплантации сосуды. Однако она решает многие важнейшие проблемы, стоящие на пути к этой цели. Ученые собираются продолжить работу и через несколько лет дойти до стадии клинических испытаний, а в итоге — и до практического применения своего подхода.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl + Enter.

